金納米顆粒摻雜的羊毛角蛋白作為新型碳前體和穩定劑來制備多孔碳。在500℃碳化溫度下,所得金摻雜多孔碳顯示出**的脫質子化性能(pH敏感性),傳感器的pH靈敏度為57 mV/pH,相對標準偏差為0.088%。在700℃碳化溫度下,所得多孔碳材料具有高度sp2結構,對尿酸的氧化表現出良好的導電性和電催化活性。尿酸傳感器在1–150 μM的范圍內具有線性響應的特性,檢測**為0.1 μM。
1.結構調控策略
在劇烈攪拌下,向5 mL羊毛角蛋白(WK)溶液(2.5wt%)中加入5 mL的HAuCl4(10×10-3 M)水溶液,調節反應物的pH至10~12,在45℃下保溫12 h,得到金納米粒子和羊毛角蛋白(AuNPs@WK)復合溶液。WK在分子水平上有利于納米結構的調控。一方面,WK通過熱處理可形成N-摻雜的芳環。另一方面,WK分子上大量的二硫鍵是羊毛纖維結構穩定的重要因素。在WK溶液的制備過程中,部分二硫鍵斷裂。每一個斷裂的二硫鍵形成兩個巰基(-SH),它們不穩定但活潑,可用作還原劑。利用這些不穩定的巰基可以將Au離子還原為Au原子,并通過強相互作用使AuNPs表面吸附WK分子,使其緊密地錨定在獨特的WK分子前體骨架中(圖2)。將經冷凍干燥制備的固體樣品在氮氣氣氛下于400至800℃碳化,得到AuNPs摻雜碳復合材料,命名為AuNPs@NPWC-400,AuNPs@NPWC-500,AuNPs@NPWC-600,AuNPs@NPWC-700和AuNPs@NPWC-800。
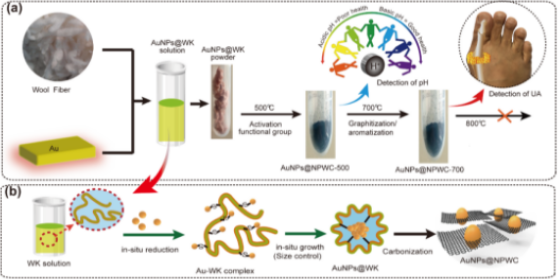
圖1. 金納米顆粒(AuNPs)摻雜多孔碳材料的制備。(a)控制制備AuNPs摻雜基于羊毛多孔碳(AuNPs@NPWC),實現不同功能與應用。在500℃碳化溫度下,吡啶、吡咯等氮含量高的石墨材料對pH傳感敏感,而在700℃碳化溫度下,材料芳構化程度高,孔隙率高,可緊密錨定且良好分散球形AuNPs,對尿酸(UA)傳感更為靈敏。(b)示意圖顯示了AuNPs的原位還原合成,以及**碳化成AuNPs@NPWC復合材料。
2.結構表征
孔隙度的大小取決于揮發性物質的釋放。復合材料中AuNPs可催化并加速前驅體堿性蛋白質向二氧化碳和氮的演化,從而擁有高孔隙率特性和改性芳香環。圖2b-f所示的TEM圖像顯示了AuNPs的形貌,在700℃的碳化溫度下觀察到尺寸范圍為20-40 nm的球形AuNPs,粒徑分布均勻,而在800℃時,發現了團聚顆粒。圖2g-k所示為TEM圖像,顯示碳化溫度對碳形態的影響,孔隙率和晶格百分比隨溫度升高而增加。在TEM成像之前,通過在乙醇中超聲處理復合樣品數小時,證實了AuNPs被牢固地錨定在多孔碳基體中。圖2l-p為碳化樣品的SEM圖像顯示,碳化溫度從400到700℃時,復合材料的孔隙率增加,而在800℃碳化溫度下,孔隙率下降。孔隙率下降是由于碳在高溫軟化后收縮,導致孔隙縮小或閉合。研究溫度對AuNPs形貌的影響,原位合成的納米顆粒在多孔碳微結構基體中分布均勻,活化溫度從400℃增加到700℃,結構和形貌沒有發生任何破壞,而在800℃下,會導致AuNPs的團聚,表面形貌破壞。X射線粉末衍射儀(XRD)圖(圖2q)表明了復合材料的結晶度。在2θ = 25.8°處,AuNPs@NPWC的衍射峰顯示了石墨晶面(002),屬于六角共軛碳結構。此外,四個較強的衍射峰對應AuNPs的(111)、(200)、(220)和(311)晶面。與粉末衍射標準聯合委員會的塊體金標準圖比較(JCPDS:65-2870),所得AuNPs的衍射峰位于同一角度,證實了AuNPs在復合材料中的形成。碳化后的拉曼光譜證實了合成的AuNPs@NPWC的sp2和復合結構(圖2r)。所有光譜都顯示出兩個**的譜帶D和G帶,D帶通常歸因于無序碳結構(例如納米管壁上的缺陷、空位、扭結和雜原子),而G帶則歸因于C-C對稱拉伸。拉曼光譜上在1360和1595 cm?1處獲得的兩個帶是AuNPs@NPWC的D和G帶。當溫度從400℃升高到700℃時,ID/IG比值從0.88增加到1.01,表明碳原子SP2結構的增多。但在800℃時ID/IG下降到0.96,表明無序結構的增加。隨著溫度的升高,碳含量增加,氮、氫含量降低。在高于700℃的碳化溫度下,C/H比幾乎沒有改變,表明化學成分沒有進一步變化。在400、500、600、700和800℃下合成的產物的比表面積(BET)分別為27.09、381.22、452.65、625.06和447.64 m2/g。孔隙率和比表面積的穩步上升的現象,與交聯反應形成的化合物有關。然而,在800℃的高溫下,比表面的下降是由于碳結構的收縮。孔隙率、芳構化程度的結果與之前觀察到的TEM和SEM結果一致。此外,用X射線光電子能譜(XPS)研究了碳化條件對復合材料化學狀態和原子構象的影響,發現C、N、O和Au元素有四個明顯的特征峰。
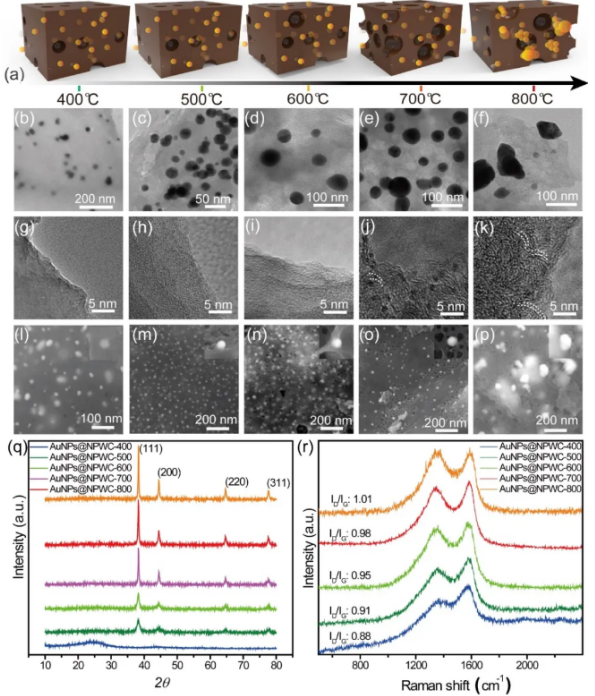
圖2. 400~800℃碳化溫度對AuNPs碳骨架和形貌的影響。(a)不同碳化溫度下AuNPs@NPWC的結構示意圖。(b-f)不同碳化溫度下AuNPs@NPWC的透射電鏡(TEM)圖像,顯示了AuNPs的形態和分散性。(g-k)TEM中顯示了碳化溫度對芳構化碳骨架的影響。(l-p)不同碳化溫度下AuNPs@NPWC的掃描電鏡(SEM)圖像和AuNPs分散性情況。(q)AuNPs@NPWC的XRD圖譜(r)AuNPs@NPWC的拉曼光譜。
3.pH傳感
利用AuNPs@NPWC-400,AuNPs@NPWC-500,AuNPs@NPWC-600,AuNPs@NPWC-700和AuNPs@NPWC-800制備了能夠檢測體液pH的雙電極柔性條傳感器(圖3a)。
具有COO-官能團的氮摻雜含碳復合材料具有芳構化碳骨架和N-摻雜結構,表現出對H+離子的高靈敏度(圖3b)。研究了所制備的傳感器在McIlvaine緩沖液pH在4至6之間的上升和下降響應(圖3c)。其中,使用AuNPs@NPWC-500的傳感器具有高靈敏度為57 mV/pH,相對標準偏差(RSD)為0.088%。我們發現復合材料的靈敏度與結構和化學性質有關。**,AuNPs@NPWC-500的表面積相當好。其次,吡啶類N1和吡咯類N2的總含量高,隨著碳化溫度的升高,開始轉移到穩定的石墨N3和氧化N4中。高含量的吡啶N1和吡咯氮對H+更敏感。此外,C-O和C=O含量的增高,減少了以二氧化碳的生成。與無AuNPs摻雜NPWC-500的電極pH響應進行了比較,AuNPs@NPWC-500傳感器的靈敏度明顯較高。在沒有AuNPs的情況下,碳化過程沒有AuNPs的催化作用,導致孔隙率降低,使比表面積降低。綜上所述,高脫質子化強烈依賴于高含量的吡啶氮和吡咯氮,以及大量的羧酸基團和良好的孔隙率,AuNPs@NPWC-500在這五種結構中具有較佳比表面積,π-共軛和N-摻雜芳香族結構組合。
對利用AuNPs@NPWC-500為工作電極條形pH傳感器進行了進一步的研究。由于人體體液中的pH值通常在3到8之間,因此對基于AuNPs@NPWC-500的pH傳感器在pH為3-8的范圍內重復測試電位,其平均斜率為52.97 mV/pH(圖3c)。當加入1mM Ca2+、1 mM NH4+、1 mM Mg2+、8 mM Mg2+、8 mM K+或20 mM Na+時,傳感器對H+離子的選擇性很高,電位變化為3.3%(圖3d)。為了研究重現性,制作了四個平行傳感器,在pH為3時絕對電位范圍為373.8到377.7mV,靈敏度在每單位濃度55.2到57 mV/pH之間變化。這些傳感器顯示的RSD為0.88%,與先前的報告相比非常小。為了用于制備標準校準曲線和測量體液(即尿液和汗液)的pH值,對pH傳感器的穩定性進行了測試,顯示8小時測量中僅有0.9 mV的偏差。體液定量分析的主要障礙是Cl-對固態Ag/AgCl參比電極的影響,本文中使用基于聚乙烯醇縮丁醛酯(PVB)的Ag/AgCl參比電極克服了這一問題,這是因為PVB層含有Cl-,并且能夠抵抗Cl-濃度的變化。以上測試結果表明,現有的pH傳感器具有準確可靠的分析能力。
通過檢測體液來研究pH傳感器的實用性,使用商用pH計(M/s. Thermo-scientific)檢測和驗證人體汗液和尿液樣本的pH值。使用傳感器對體液的定量測試是通過從緩沖溶液的潛在值獲得的校準曲線計算而來的。為了進行真實樣本分析,收集了志愿者5份汗液和5份尿液樣本。所制備pH傳感器測量的汗液和尿液的pH與商用pH計所測值相比,**變化為0.72%和2.09%。這些差異與體液的正常pH值范圍相比相對較小。
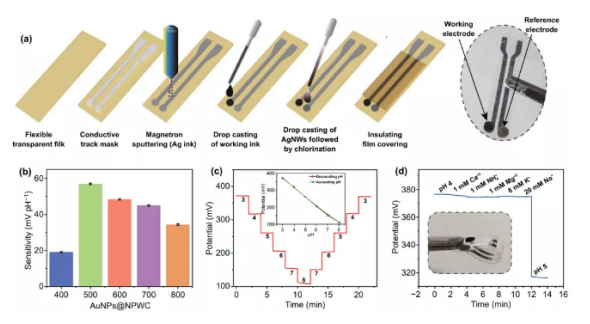
圖3. pH傳感器的設計和性能:(a)條狀雙電極柔性傳感器的制備;(b)碳化復合材料傳感器的pH靈敏度;(c)重復性分析;(d)AuNPs@NPWC-500傳感器的選擇性(插圖顯示傳感器的彎折性能)。4. UA傳感
制備了UA傳感器,所得材料用于UA檢測顯示出高電催化活性,具有高的靈敏度和選擇性。在水溶液中,UA在催化劑修飾的電極上容易被氧化釋放電子。我們的非酶電催化測試表明帶有金屬納米粒子的碳化材料AuNPs@NPWC由于sp2雜化碳結構和零禁帶,是UA電催化氧化的較佳非酶電催化材料(圖4a)。
制備了三電極柔性條基電催化系統,用于測定水介質中的UA濃度,該體系具有工作電極、Ag/AgCl參比電極和對鉑電極(圖5b)。**,利用在不同溫度下碳化材料(AuNPs@NPWC-400,AuNPs@NPWC-500, AuNPs@NPWC-600, AuNPs@NPWC-700, AuNPs@NPWC-800)制備了五種不同工作電極的傳感器。圖4c為使用不同傳感器在0.1 mM UA含磷酸鹽緩沖液(pH = 7)中獲得的伏安圖。結果表明,AuNPs@NPWC-700傳感器與其他相比具有較高的峰值電流。AuNPs@NPWC-700具有較高孔隙率(比表面:625.0586 m2/g)、更多的芳環化結構(圖2i,p和q),以及(1d,n)良好的AuNPs分布,因此對UA的氧化表現出**的電催化性能。AuNPs@NPWC-800由于比表面減小(447.6388 m2/g)并發生AuNPs的團聚和形貌破壞(圖3e和o),因此相應的傳感器對UA催化氧化較慢。從所有碳化樣品反卷積XPS光譜來看,C1s光譜顯示C=C含量隨溫度升高而增加,表明石墨化程度很高,會增強電流響應。反卷積的N1s光譜顯示石墨氮的百分比隨溫度的增加而增加,在平面上摻雜N有助于錨定AuNPs,并改善電流響應。AuNPs@NPWC-700電極在1 mM UA情況下的伏安圖顯示UA的氧化峰(圖4d)。
微分脈沖伏安法(DPV)在-0.2~1 V的電位范圍內進行,在PBS(pH = 7.0)溶液中測試出UA的氧化峰電位在0.22 V處(圖4e)。峰值電流與UA濃度之間的線性響應范圍為1 μM至150μM,檢測限為0.1 μM(S/N = 3)。據我們所知,AuNPs@NPWC-700電極的線性范圍優于先前報道的UA檢測的金屬納米粒子復合碳基電極。30天后AuNPs@NPWC-700傳感器氧化峰值電流值為**天的90.15%,顯示出高穩定性和長期耐用性。**的穩定性歸因于無電催化材料的破壞,從SEM中也可以看出電極材料在使用前后沒有明顯變化。在-0.25~0.75 V電壓范圍內,使用Ag/AgCl參比電極進行了干擾實驗,篩選出可能的干擾物質:葡萄糖(0.1 mM)、抗壞血酸(0.1 mM)、尿素(0.1 mM)和乳酸(0.1 mM)。除尿酸外,其他可能的干擾物質沒有記錄到明顯的峰,這表明所制備的AuNPs@NPWC-700電極對尿酸的選擇性催化氧化性能好。
所研制的生物傳感器具有較高的準確度和效率。所得條形傳感器和商用UA傳感器在室溫下對人類尿液樣本中UA濃度之間的相關曲線如圖5f所示,并給出了生物傳感器對UA濃度響應的校準曲線。在實際樣本分析中,采取了10份來自志愿者的尿樣,并用PBS(pH = 7)以1:50比例稀釋。使用DPV分析每個稀釋樣品的電流響應,并使用校準曲線圖4e(插圖)計算UA的濃度。所制傳感器(X軸)和商用UA檢測器(Y軸)檢測的UA濃度(圖4f)的相關系數為0.9767。
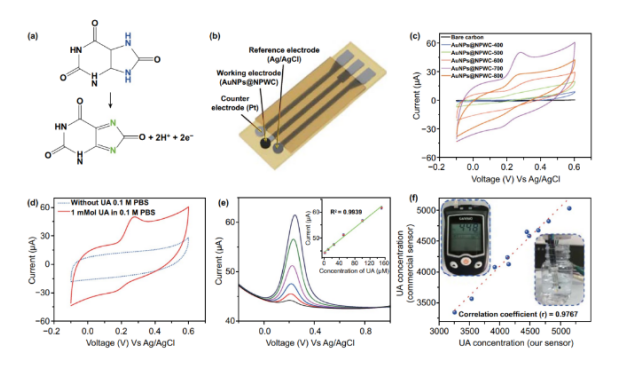
圖4. UA傳感器的設計和性能:(a)非酶電催化UA氧化反應。(b)條形三電極柔性傳感器示意圖。(c)使用不同材料電極在1.0 mM UA的PBS(0.1 M,pH=7)溶液中的循環伏安圖。(d)AuNPs@NPWC-700電極在含有1.0 mM UA和不含UA的PBS(0.1M,pH=7)溶液中的循環伏安圖。(e)AuNPs@NPWC-700電極在不同濃度的UA(1–150 μM)的PBS(0. 1M pH=7)溶液中的差示脈沖伏安(DPV)曲線。相應氧化電流與UA濃度的關系圖(插圖)。(f)所研制的生物傳感器與商業標準UA計的性能相關性。
我們有零維/一維/二維/三維四個分類來提供幾十個產品分類和幾千種納米材料,材料的材質包含金屬納米材料和非金屬納米材料以及他們的氧化物或碳化物及復合定制等等,粒徑從5納米-2000納米均可選擇。
相關產品
離子液體包裹納米金修飾
碳包裹納米金屬粒子
高分子脂質體包裹的納米金(LADL@Au NPs)
介孔二氧化硅包裹的正電荷納米金
聚乙烯亞胺/聚乙二醇修飾納米金顆粒
負載釓釓螯合劑DOTA-NHS的樹狀大分子包裹的納米金顆粒
環糊精修飾的樹狀大分子包裹的納米金
聚乙二醇化樹狀大分子包裹的納米金顆粒
RGD多肽修飾的多功能樹狀大分子包裹的納米金顆粒
透明質酸包裹的金納米粒子
殼聚糖包裹納米金粒子
泛影酸/葉酸修飾的多功能樹狀大分子包裹的納米金顆粒Au DENPs
靶向脂質體包裹水相納米金復合物
殼聚糖改性聚氨酯及殼聚糖包裹納米金
葉酸修飾的多功能靶向造影劑磁性氧化鐵/金納米顆粒
葉酸修飾的復合泛影酸的聚酰胺-胺樹狀大分子金納米粒子
檸檬酸根包裹的納米金顆粒
金納米顆粒功能化二硫化鉬納米復合材料
溶菌酶功能化金納米顆粒材料
魯米諾及衍生物功能化的金納米材料
DNA功能化的金納米顆粒
苝酰亞胺功能化的金/銀納米顆粒
杯芳烴功能化金納米顆粒
賴氨酸修飾的苝酰亞胺功能化金納米顆粒
多層殼包覆的功能化金納米顆粒
乳糖酸修飾的低代數PAMAM包裹金納米顆粒
硫辛酸功能化的金納米顆粒
樹枝化聚苯/金復合納米粒子
功能化Pd@Au納米顆粒
抗氧化配基功能化的金納米復合物
功能化金剛石納米顆粒
多肽功能化金納米顆粒
納米金顆粒包裹的PEG功能化PAMAM樹狀大分子
金納米顆粒修飾的硫酚功能化石墨烯復合材料
葉酸修飾的多功能靶向造影劑磁性氧化鐵/金復合納米顆粒
三聯吡啶衍生物配體與β-二酮稀土配合物包覆金納米顆粒
金納米顆粒修飾的多壁碳納米管(MWCNTs)
多官能團表面修飾金屬納米顆粒
碳納米管/聚苯胺/納米金復合材料
配位鍵修飾的功能性納米顆粒/氧化石墨烯納米雜化材料
牛血清白蛋白修飾納米金顆粒
金納米顆粒功能化還原氧化石墨烯(RGO)和多壁碳納米管(MWCNTs)
鉑修飾的枝狀金納米復合材料
C18鍵合納米金修飾二氧化硅顆粒
石墨烯(GS)-殼聚糖(CS)-納米金(Nano-Au)復合材料
納米金(Au)包被瘦肉精-牛血清蛋白(CLB-BSA)
納米金修飾羧甲基殼聚糖
納米金修飾乙酰膽堿酯酶
柔紅霉素修飾的納米金
金納米顆粒復合材料(ssDNA-AuNPs);Hyaluronic Acid-DNA透明質酸修飾脫氧核糖核酸
二氧化硅包裹金納米顆粒
氨基、羧基功能化的納米金試劑
PEG包裹的納米金顆粒(PEG末端鏈接不同基團)
BSA包裹的納米金顆粒
葡聚糖包裹的納米金顆粒
氨基功能化的金納米粒子
羧基功能化的金納米粒子
聚乙烯亞胺包裹納米金(PEI-nanogold)
氧化氣氛下氧化鈦包裹金納米顆粒
金納米離子包裹二氧化硅殼核材料
紅細胞膜包被金納米顆粒
11-巰基十一烷酸包裹的金納米顆粒
單分散性PEG修飾金納米顆粒
納米金顆粒標記外泌體
葡萄糖包被的納米金顆粒(Gold Nanoparticle, GNP)
納米金顆粒標記外泌體
氧化硅修飾的納米金
D-丙氨酰-D-丙氨酸(D-alanyl-D-alanine,DADA)修飾金納米顆粒(Au_DADA)復合材料
四面體DNA修飾金納米顆粒上合成Au-TDNNs復合材料
精氨酸/氨基酸修飾金納米顆粒
富勒醇修飾的金納米顆粒
肽修飾的金納米顆粒
FITC/羧基官能化修飾金納米顆粒
CY3/FITC/馬來酰亞胺功能化金納米顆粒
CY3和羧基官能化金納米顆粒
FITC和疊氮功能化金納米顆粒
Cy3和NHS功能化金納米顆粒
FITC和甲基功能化金納米顆粒
FITC和生物素功能化金納米顆粒
Cy3和蛋白A功能化金納米顆粒
zzj 2021.3.17




 齊岳微信公眾號
齊岳微信公眾號 官方微信
官方微信 庫存查詢
庫存查詢