對于蛋白活性的**控制一直是生物工程領域的熱門話題,尤其是在生物系統內控制蛋白質的技術更是用途甚廣。在過去的十年中,已經有一些技術在這一領域初有建樹,包括的光遺傳技術(optogenetics),發光基團輔助光失活(chromophore-assisted light inactivation,CALI),以及合成分子光開關(synthetic photoswitches)。這些手段地促進了人們對于蛋白質功能的理解,并在生物領域產生了重大影響。然而,目前大多數的技術嚴重地依賴于基因編輯。這使得它們在醫學轉化方面的前途受到影響。因此,一種分子熱療技術將為此領域帶來重要進展。
分子熱療技術的介紹:
簡單地說,熱療是通過升高部分組織的溫度來引起特定組織凋亡而不傷及其他區域的手段。從傳熱學的角度,熱的傳導范圍與時間息息相關。因為的尺寸較大,傳統熱療至少需要幾分鐘的時間,以創造范圍足夠大的溫度場殺死。借用熱療的概念,如果能將加熱的時間縮短至納秒,同時提高能量密度,我們就可以創造出,甚至納米尺度的高溫場用以滅活特定蛋白而不傷害細胞。因為加熱尺度與分子尺度接近,這種技術被稱為“分子熱療”。分子熱療需要將金納米顆粒與目標蛋白相連接,在納秒脈沖激光的照射下,金納米顆粒會產生足夠高的局域高溫場使目標蛋白滅活而不會造成細胞凋亡。
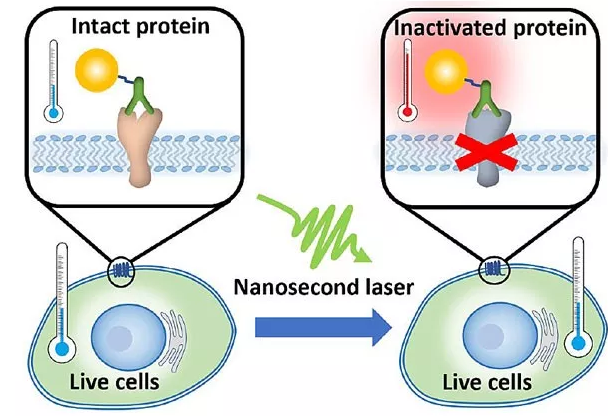
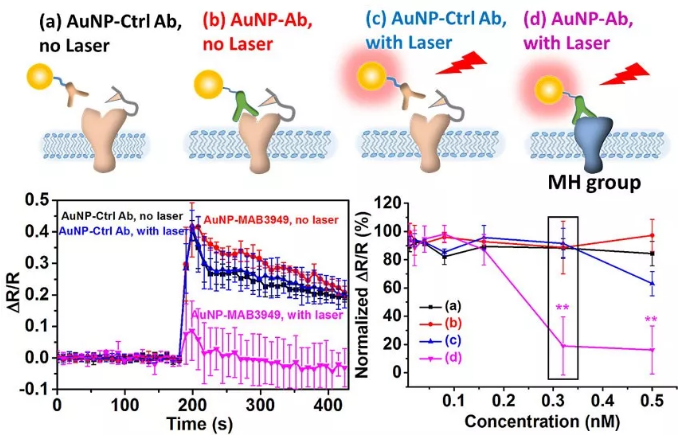
**,我們對分子熱療的性在溶液環境下進行了測試。測試發現通過胰凝乳蛋白酶連接于金納米顆粒表面,納秒激光脈沖能夠**的滅活連接在金納米粒表面的蛋白酶而不會造成溶液整體的溫度提升,通過對分子熱療中納秒時域的蛋白滅活行為進行分析,發現高溫下蛋白分子的去折疊反應動力學與低溫時傳統的Arrhenius model有著明顯的區別,接著,分子熱療被用于活細胞膜蛋白的滅活。通過表面修飾抗體,金納米顆粒可以特異性地連接于細胞表面的蛋白酶激活受體2(Protease activated receptor 2, PAR2)。在進行激光脈沖照射之后,連接有金納米顆粒的細胞的PAR2活性相較于對照組下降明顯。PAR2的失活會維持4個小時左右,而后緩慢恢復。重要的是,細胞活性并不會因為分子熱療產生明顯下降,這證明了分子熱療對于細胞的安全性。最后,另一種膜蛋白-連接黏附分子A (Junctional adhesion molecule A,JAM-A)也被證明可以被分子熱療滅活。并且JAM-A的滅活會引發體外血腦屏障模型的打開。因此分子熱療將有可能發展成一種開啟血腦屏障的手段。
西安齊岳生物**供應各種來源的細胞膜。包括紅細胞膜;白細胞膜;血小板細胞膜;細菌細胞膜;細胞膜;干細胞膜;原代細胞膜;各種細胞系膜 上皮細胞膜;成纖維細胞膜;生物膜。
溫馨提示:西安齊岳生物提供的所有產品僅用于科研,axc.2021.01.28




 齊岳微信公眾號
齊岳微信公眾號 官方微信
官方微信 庫存查詢
庫存查詢